
Haber Merkezi Ankara / 14 Aralık 2025
-Ruhsat yok → Çünkü Acil Kullanım İzni Varmış!
Haber merkezimiz, Rüya ASLANTEPE’nin paylaşımının hemen ardından konuyu araştırmaya başlamıştır. Bu kapsamda ASLANTEPE’ye mesaj gönderilmiş, ayrıca “T.C. Sağlık Bakanlığı – Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK)” tarafından verildiği belirtilen belgeyle ilgili olarak Sağlık Bakanlığı ile irtibata geçilmiştir. Ancak haberin yayına hazırlandığı saate kadar ne ASLANTEPE’den ne de Sağlık Bakanlığı’ndan herhangi bir geri dönüş alınamamıştır.

ASLANTEPE’nin paylaşımında dikkat çeken en önemli hususlardan biri, “BIONTECH TURKEY TIBBİ ÜRÜNLER VE KLİNİK ARAŞTIRMA TİCARET ANONİM ŞİRKETİ” nin 12 Mart 2021 tarihinde kurulmuş olmasıdır. (Kurulan şirkette Türk yok!)
Şirket bilgileri aşağıda olduğu gibidir.

Buna karşılık, 18 Mart 2021 tarihinde Türkiye’ye ilk 4,5 milyon doz Pfizer-BioNTech mRNA sıvısının sevkiyatı ve depolama işlemleri yapılmıştır.
2 Nisan 2021 tarihinde ise Sağlık Bakanı’nın açıklamasına göre BioNTech sıvısı Ankara’da uygulanmaya başlanmıştır.

Yani kronolojik olarak;
- Önce şirket kurulmuş,
- Yalnızca 6 gün sonra BioNTech mRNA sıvısının alım süreci başlamış,
- Ardından bu sıvı Türkiye genelinde uygulanmıştır.
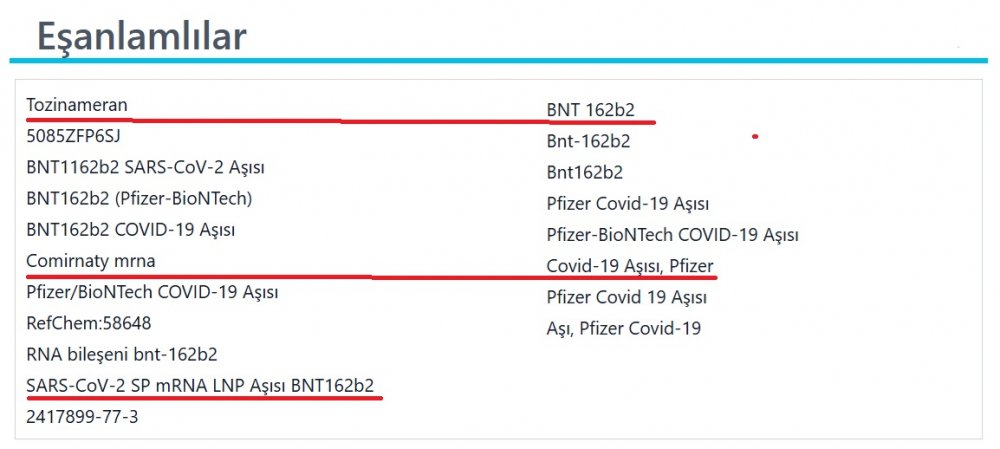
Tozinameran ve Comirnaty Nedir?
Bakanlığın mahkemeye sunduğu belgelerde yer alan, Tozinameran ve Comirnaty kavramlarına açıklık getirilmesi gerekmektedir. Zira ancak bu şekilde, söz konusu mRNA sıvılarıyla ne yapıldığı ve hangi kapsamda kullanıldığı daha net anlaşılabilecektir.
Tozinameran, Pfizer-BioNTech COVID-19 aşısının (BNT162b2) etken maddesidir.
Comirnaty ise bu aşının ticari adıdır.
Bu aşı, Pfizer ve BioNTech iş birliğiyle yürütülen “Project Lightspeed” kapsamında geliştirilen mRNA bazlı aşıdır. Aşı, SARS-CoV-2 virüsünün spike (S) proteininin optimize edilmiş tam uzunluktaki versiyonunu kodlayan nükleozid modifiye mRNA (modRNA) içermektedir.
ModRNA:
- Lipid nanopartiküller (LNP) içinde formüle edilir,
- Üç hafta arayla iki doz hâlinde,
- İntramüsküler enjeksiyon yoluyla uygulanır.
Comirnaty;
- ABD (NCT04368728) ve Almanya (NCT04380701) klinik çalışmalarında değerlendirilmiş,
- 13 Temmuz 2020’de ABD FDA tarafından “Hızlı Yol (Fast Track)” statüsü almış,
- 11 Aralık 2020’de FDA tarafından Acil Kullanım Yetkisi (EUA) verilmiştir.
- 2 Aralık 2020’de Birleşik Krallık’ta,
- 9 Aralık 2020’de Kanada’da acil kullanım onayı almıştır.
- Tam FDA onayı ise 23 Ağustos 2021 tarihinde verilmiştir.
Buna rağmen, ruhsatı olmayan bu sıvıların, uzun dönem koruyuculuk ve bulaşmayı önleme konusunda yeterli verinin henüz mevcut olmadığı, kendi resmi dokümanlarında da belirtilmiştir.
Tozinameran’ın Teknik Tanımı
Tozinameran;
SARS-CoV-2 spike glikoproteininin optimize edilmiş formunu kodlayan nükleozid modifiye mRNA’yı kapsülleyen lipid nanopartikül (LNP) formülasyonudur.
Enjeksiyon sonrası:
- LNP’ler hücre zarına bağlanır,
- mRNA hücre içine girer,
- Hücresel protein sentez mekanizması spike proteinini üretir,
- Bu durum bağışıklık sisteminde antikor ve T-hücre yanıtı oluşturur.
Famtozinameran Nedir?
Bir diğer dikkat çekici unsur ise Famtozinameran’dır.
Famtozinameran, daha düşük dozlu ve modifiye edilmiş bir mRNA formu olarak tanımlanmaktadır.
Sağlık Bakanlığı’nın mahkemeye sunduğu belgelerden anlaşıldığı kadarıyla:
- İki farklı Pfizer-BioNTech mRNA formu (Tozinameran ve Famtozinameran) söz konusudur.
- Ancak bu sıvıların:
-Ne kadar alındığı,
-Hangi illere gönderildiği,
-Kimlere uygulandığı konularında herhangi bir resmi veri bulunmamaktadır.
Bu kadar kritik bir ayrıntının mahkeme belgesinde yer alıp, kamuoyuna açık biçimde açıklanmamış olması anlaşılır değildir.
Ruhsat Meselesi
Sağlık Bakanlığı kayıtlarında şu ifade yer almaktadır:
“Usulden veya esastan iptal edilen ya da reddedilen bir ürün bulunmamaktadır.
Pfizer PFE İlaçları A.Ş.’nin COVID-19 aşısına ilişkin herhangi bir ruhsat başvurusu yapılmamıştır. Kurumumuzca ruhsatlandırılmış bir COVID-19 aşısı bulunmamaktadır.”
Bu ifade, BioNTech-Pfizer COVID-19 aşılarının ruhsatlı değil, yalnızca “Acil Kullanım İzni” kapsamında kullanıldığını teyit etmektedir.
ASLANTEPE’nin Sorusunun Cevabı;
Rüya ASLANTEPE’nin şu sorusu dikkat çekicidir:
“Şayet Sağlık Bakanlığı Pfizer-BioNTech’ten bu aşıları temin etmediyse, kimden tedarik etti ve hiç ruhsat vermediyse — ki vermemiştir, mahkeme tutanaklarında da sabittir — 86 milyon Türk milletinin canı nasıl hiçe sayılmıştır?”
Bu soruda bahsi geçen Pfizer-BioNTech COVID-19 aşısı,
BNT162b2 / Tozinameran / Comirnaty olarak bilinen mRNA sıvılarıdır.
Bu sıvılar için:
- Ruhsat verilmemiştir (doğru),
- Acil Kullanım İzni, Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK) tarafından verilmiştir.
Ancak dikkat çekici olan nokta şudur:
Bu sıvılar doğrudan Pfizer-BioNTech’ten değil, 12 Mart 2021’de kurulan “BIONTECH TURKEY TIBBİ ÜRÜNLER VE KLİNİK ARAŞTIRMA TİCARET A.Ş.” üzerinden temin edilmiştir.
Sonuçta Rüya ASLANTEPE’nin paylaşımında asıl sorgulanması gereken hususlar şunlardır:
1-Şirketin kuruluş tarihi ve yapısı,
2-Şirket tüzüğüne sonradan Sağlık Bakanlığı temsilcisinin dahil edilmesi,

3-Tozinameran ve Famtozinameran alımlarının, miktarı ve dağıtım (varsa kayıtları) alanları,
4-Ve tüm bu süreçlerin neden şeffaf biçimde kamuoyuna açıklanmadığı.
Varsa elbette.

























5gvirusnews haber yaparsa böyle yapar. Bu paylaşımın Facebook da hounve hemen sayfanıza baktım